Un mécanisme qui agit au niveau moléculaire pour aider le virus herpès simplex (HSV1) à infecter le cerveau a été découvert par une équipe de chercheurs de l’université d’Aarhus, de l’université d’Oxford et de l’université de Göteborg, dirigée par Chiranjeevi Bodda, le premier auteur de l’étude publiée dans le Journal de la médecine expérimentale.
Ce virus peut infecter les cellules épithéliales et peut se propager des nerfs périphériques au système nerveux central, puis au cerveau. Elle peut y provoquer une encéphalite et une mortalité relativement rare mais élevée si elle n’est pas traitée à temps. Dans la plupart des cas, cependant, le système immunitaire empêche à lui seul l’infection du cerveau, mais dans certains cas, le virus peut échapper à ces systèmes de défense et infecter le cerveau.
Le virus active les stimulateurs de gènes de l’interféron (STING), un mécanisme de défense du système immunitaire, au cours de l’infection et le STING déclenche à son tour diverses actions cellulaires pour combattre l’invasion. Ces actions comprennent la production de cytokines telles que l’interféron de type I (IFN).
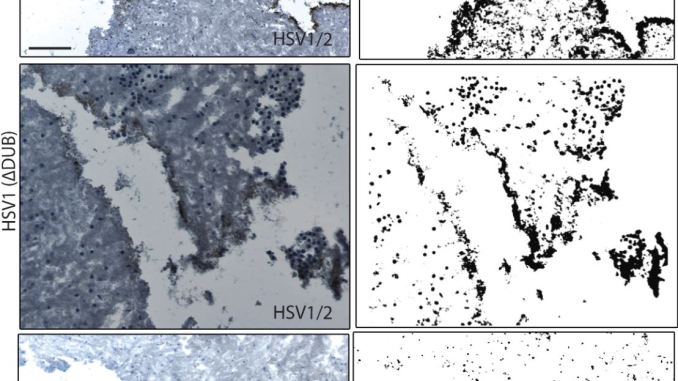
Comme l’explique M. Bodda, on n’avait jamais compris comment le HSV1 parvient à surmonter les dispositions de l’IFN de type I dans le cerveau. Les chercheurs ont donc réalisé des expériences sur des cellules cérébrales de souris en culture en découvrant un gène du virus, appelé VP1-2, qui, une fois muté, semblait supprimer l’immunité.
Le gène muté n’avait pas la capacité d’effectuer une modification post-traditionnelle appelée ubiquitine.
“Notre étude montre que le HSV1 cible l’ubiquitination de STING dans le cerveau pour favoriser l’infection virale et la progression potentielle vers l’encéphalite herpétique simplex”, explique encore M. Bodda. “Un médicament qui inhibe la capacité du virus à éliminer l’ubiquitine pourrait permettre aux cellules du cerveau de déclencher une réponse antivirale efficace contre le HSV1. Cela pourrait être particulièrement bénéfique pour les patients immunodéprimés souffrant d’une grave infection cérébrale au HSV1, notamment dans les cas qui résistent au traitement standard à l’acyclovir”.